Actividad física o ejercicio - ¿Cuál es mejor para vivir saludable?
Más de 15,000 científicos, médicos y otros profesionales de la salud se acercaron a Boston para las Sesiones Científicas Anuales de la ADA este año, el 759999º aniversario de esta conferencia gi-normous dirigirse a nuevas investigaciones en cuidado y tratamientos de la diabetes. El festival de ciencia de este año contó con más de 385 presentatio ns y más de 2, 300 pósters de investigación, incluidos 60 acompañados por "recorridos de audio" que los asistentes pueden escuchar (¡visita a un museo sagrado!)

Toda una sección expansiva de la sala de exposiciones está bloqueada para el increíble laberinto de carteles de investigación, que se muestran en divisores que parecen paredes corporativas de cubículos. Como si todo esto no fuera suficiente, parece que no hay fin en los simposios de compañías preprograma (asuntos de desayuno y cena), fiestas fuera de horario, recepciones y reuniones. Para la comunidad en línea de Diabetes, hubo recepciones especiales este año organizadas por la propia ADA, Medtronic, Johnson & Johnson, Sanofi, Eil Lilly y Novo Nordisk.
¡Uf! Me canso solo de explicarlo.Medtronic
Medtronic tuvo un fin de semana histórico con cuatro anuncios de noticias, catapultando a la bomba de insulina y la empresa CGM a la luz pública.

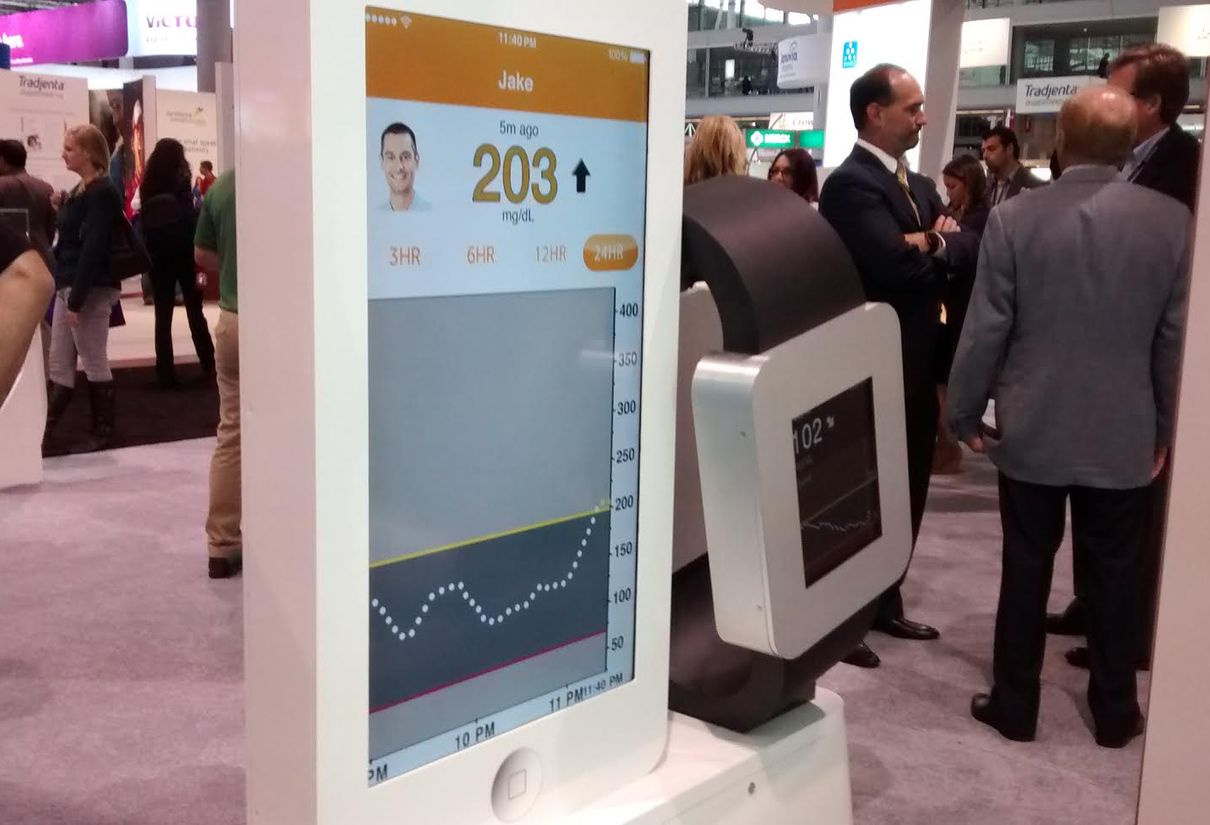
El viernes, la compañía anunció que había obtenido la aprobación de la FDA a mediados de mayo de lo que llama Minimed Connect, un nuevo sistema de intercambio de datos para su bomba de insulina combinada y CGM. Para usarlo, necesitas un pequeño dispositivo Uploader que se puede llevar en el bolsillo o en un llavero (ese doohicky negro representado entre la bomba y el iPhone), que transmite datos en tiempo real de una bomba Paradigm Revel o 530G con un sensor Enlite CGM al sistema Minimed CareLink en línea. Esto se facilita a través de una aplicación para teléfonos inteligentes (actualmente solo está disponible para iPhone, pero próximamente llegará Android) que también entrega mensajes de texto preestablecidos a sus seres queridos o padres para Altos o Bajos. (Aquí está la documentación de la FDA, por cierto).
Tenemos que manejar el cargador ligero en el stand de la compañía, y Mike (un camión de bomberos de Medtronic) dice que definitivamente podría verse cortándolo con facilidad en sus llaves.

El cargador cuesta $ 199 y estará disponible a partir del otoño, con un pre-pedido a partir de julio, dice la portavoz de Medtronic, Amanda Sheldon.
Ligado a eso, Medtronic anunció que se está asociando con Samsung y Glooko. Lo que esto significa es que el sistema pronto transmitirá datos directamente a los smartwatches de Samsung (utilizando un sistema operativo Tizen basado en Linux). Tenemos que admitir que la interfaz de usuario en ese reloj, con su cara curva, se ve muy dulce! Y pronto los usuarios de Medtronic podrán ver y compartir sus datos en la plataforma Glooko, que es enorme, especialmente para aquellos que les gustan los dispositivos de Medtronic pero que no son fanáticos de su sistema de software propietario, CareLink.

En noticias (casi) más grandes, Medtronic anunció que está lanzando la primera prueba pivotal para su sistema híbrido de ciclo cerrado (también conocido como 670G), que es un páncreas preartificial que aún requiere alguna intervención del usuario (es decir, no completamente automatizado). Esto es GRANDE porque es el primer "ensayo pivotal" de tecnología de ciclo cerrado realizado en los EE. UU. En investigación, un ensayo "pivotal" es el último que proporciona evidencia de que un medicamento o dispositivo está listo para el mercado. ¡Con esto, Medtronic está allanando el camino para la comercialización de un sistema AP pronto!
El primer paciente se inscribió en esa prueba, que reclutará hasta 150 personas entre 14 y 75 años de nueve regiones en los Estados Unidos y una en Europa. El estudio se extenderá hasta mayo de 2016, y esperamos que para fines del próximo año veamos una presentación ante la FDA. Se pueden encontrar más detalles sobre el ensayo en ClinicalTrials. gov (identificador: NCT01857973).

Por supuesto, antes de que el híbrido de circuito cerrado llegue al mercado, esperamos ver la disponibilidad en EE. UU. Del Minimed 640G, con su característica predictiva de suspender la glucosa y (finalmente) un diseño nuevo y más inteligente. Se lanzó fuera de los EE. UU. A principios de este año, y el ensayo clínico necesario para la revisión de la FDA está en marcha.
Y eso no es todo. La compañía también anunció una asociación con BD (Becton Dickinson) para llevar a los pacientes el nuevo conjunto de infusión FlowSmart que tendrá un catéter pequeño con puerto lateral extra diseñado para mejorar la administración de insulina y ayudar a prevenir oclusiones no detectadas.Curiosamente, BD es el jugador líder en dispositivos de inyección y agujas, pero nunca antes han hecho un set de infusión. El conjunto FlowSmart anunciado el mes pasado se utilizará ahora en las bombas Medtronic (y eventualmente en sistemas de circuito cerrado) a partir de finales de 2017 o principios de 2018.
¡Apoyos a Medtronic para muchos desarrollos emocionantes!
Insulet / OmniPod
Este es el aniversario de 10 años para Insulet y Pod, por lo que la compañía del área de Boston derrochó dos stands de Exhibit Hall, uno mostrando su historial (
40 millones de Pods hecho hasta la fecha!

) y mostrando sus alianzas de intercambio de datos con Glooko y Tidepool, y el otro un producto de exhibición directa mostrando el producto actual y una vista previa de su PDM de próxima generación. (Irónicamente, el stand de Tandem Diabetes estaba entre las dos cabinas de Insulet. Guau, ¿quién organizó eso, nos preguntamos …?) Con respecto al nuevo PDM, se ve bastante impresionante; el diseño es tan iPhone-ish, de hecho, que puede confundirlo con lo real. Los grandes cambios son:
pantalla táctil a color con navegación súper fácil
pantalla de inicio orientada a la acción con solo tres barras de comandos principales
- IOB (insulina a bordo) mostrada en la pantalla de bloqueo < contiene la base de datos de carbohidratos de Calorie King, con toneladas de información sobre alimentos comunes envasados y restaurantes
- permite 0% períodos basales templados (que dicen que es grande para uso pediátrico)
- incluso hay una ilustración de un cuerpo en el PDM con marcas para ayudarlo a rastrear sus sitios de infusión, para una buena rotación
- está habilitado para Bluetooth LE, permitiendo el intercambio de datos con Dexcom y el software y los socios de la aplicación
- Pero, para mantener el factor de forma delgado, han cambiado a una batería de litio, por lo que el nuevo PDM deberá estar enchufado (con un cable mini USB) y recargarse cada 4 5 dias.
- Sí, funcionará con los grupos existentes, por lo que no es necesario cambiar esos suministros. Pero cambiará a las tiras de prueba FreeStyle Lite. Los ejecutivos de Insulet nos dicen que planean enviar este nuevo PDM para su revisión por la FDA a fines de diciembre de 2015.

Oímos por casualidad una conversación entre un ejecutivo de Insulet y un grupo de endos pediátricos sobre la necesidad de una característica "Find Your PDM" similar a las usadas para encontrar el iPhone o las llaves de su auto si extraviarlos. ¿No sería eso una gran característica para el nuevo PDM? ! Esperamos que lo hagan.
Dexcom
En su stand, Dexcom promocionaba orgullosamente su sistema SHARE con gigantescos iPhones, relojes inteligentes y receptores G4. Por supuesto, la charla sobre cómo Dexcom envió su sistema G5 directo al teléfono inteligente a la FDA a principios de año y está en espera de aprobación.
Apenas unos días antes de la conferencia, Dexcom tuvo dos anuncios emocionantes: obtuvo la aprobación inicial de una aplicación de Android para el intercambio de datos de CGM, y firmó un acuerdo con Bigfoot Biomedical, una empresa de ciclo cerrado, que permite El intercambio de datos CGM será entretejido en su futuro sistema de Páncreas Artificial. Esto llegó justo una semana después de que Bigfoot adquirió todos los activos y patentes de diseño de la ahora extinta bomba Asante Snap.
Aunque este gran cartel saludó a los asistentes en la entrada principal de la sala de exposiciones, no había tanta expectación acerca de Afrezza de Sanofi como era de esperar, dado que es una de las nuevas opciones de tratamiento más emocionantes recientemente FDA aprobado y lanzado (¡es la primera insulina no invasiva comercialmente viable, por el amor de Dios!)
Francamente, esperaba que Afrezza fuera la droga enyesada en los autobuses lanzadera de la convención este año, pero no, eso parecía ser mayormente Invokana nuevamente, como el año pasado.
Afrezza estaba cubierto en un "Teatro de productos" el sábado por la mañana. Esta fue una introducción médica muy, seca del medicamento, que debido a las regulaciones tuvo que comenzar con la larga lista de posibles riesgos y desventajas. A pesar de que la sesión era una casa bastante abarrotada de unos 180 médicos, supongo, ciertamente no fue inspirador en ningún momento de la imaginación.
Y parece que la única otra presentación en Afrezza en esta conferencia fue un simposio patrocinado por la empresa CME (educación médica continua) celebrada el domingo por la noche. Me hubiera encantado haber sido una mosca en la pared en ese momento.

El "bajo perfil" de Afrezza fue corroborado por el destacado endocrinólogo Dr. Irl Hirsch cuando me encontré con él en la sala de altavoces de la ADA. Nos encogimos de hombros acerca de cómo Afrezza no parece estar recibiendo una sacudida justa (vea el artículo de LA Times sobre el mismo tema, y un analista que comenta que la distracción de la conferencia de la ADA en sí misma puede ser una razón por la que las recetas de Afrezza están entrando tan lentamente, ¡qué irónico!). Los observadores están conteniendo la respiración para ver cómo parece que la próxima campaña publicitaria del consumidor afecta las ventas de Afrezza.
Cuando me reuní con los ejecutivos de Sanofi, pude preguntarles directamente y me dijeron que hasta ahora ha habido tres barreras para el éxito de Afrezza:
Los médicos no han oído hablar de la insulina inhalable durante varios años (y persisten) los recuerdos del fiasco de Exubera no ayudan)
El requisito de una prueba de función pulmonar es un impedimento: los médicos tienen que averiguar a dónde derivar a los pacientes para esto, o decidieron ahorrar aproximadamente $ 600 para obtener su propia máquina < El reembolso es una lucha, ya que Medicare y los otros Pagadores ya tienen uno o más productos preferidos de insulina de acción rápida en sus formularios, por lo que Afrezza está siendo transferida a un nivel inferior (lo que significa que no está cubierto)
Sanofi planea para comenzar una campaña de publicidad para el consumidor hacia fines de este año que se centrará en los medios digitales e impresos, pero no en los anuncios televisivos, según Andrew Purcell, Jefe de la Unidad de Negocio de Diabetes en Sanofi. Esperan "demostrar éxito" primero con el medicamento, y para entonces, el nuevo cartucho de 12 unidades también estará disponible (aunque personalmente estaría más entusiasmado con la opción de 2 unidades).
- Mientras tanto, Sanofi
- estaba
- haciendo un gran impacto sobre su nueva insulina Toujeo de acción prolongada, con un perfil más suave y una incidencia de hipoglucemia aún menor que su líder de mercado, Lantus. Estaban presentando una gran cantidad de datos positivos sobre Toujeo, que viene en un bolígrafo Solostar similar al de Lantus, pero ajustado especialmente para que este producto lleve 450 unidades. Y el gran problema es que están implementando un nuevo programa de entrenamiento (Toujeo COACH), en el que los pacientes reciben capacitación personalizada y llamadas de seguimiento opcionales y correos electrónicos de una enfermera o CDE. ¡Bonito! ¿A quién no le gusta un poco la mano con una nueva herramienta para la diabetes? Escuchamos que la compañía acaba de anunciar la extensión de este programa COACH a Afrezza también: ¡muy necesario y genial! Mientras tanto, nos aseguran que no están abandonando a Lantus, por médicos y pacientes que permanecen leales a esa droga.
Alrededor de la sala de exposiciones
Como hemos notado antes, el alcance de la sala de exposiciones parecía más pequeño que en años anteriores. Sin embargo, los números cuentan una historia diferente: 136 vendedores en comparación con 120 el año pasado, pero 155 el año anterior. Notablemente ausentes en 2015 fueron Roche Diabetes y Abbott Diabetes, que presumiblemente determinaron que ex hibitar aquí ya no vale la pena su dinero. Pero escuchamos algunas cositas sobre ambas compañías durante la conferencia e incluso en nuestro propio D-Data ExChange el viernes.
Roche:
Los detalles no están completamente desarrollados, pero comprendemos que Roche planea lanzar un nuevo medidor en agosto que será el primero de su tipo en establecer un estándar para la interoperabilidad. Suena intrigante …

Word dijo que Abbott está "muy entusiasmado" con su sistema FreeStyle Libre FGM (Flash Glucose Monitoring) que ahora está disponible en el extranjero, y muchos creen que no pasará mucho tiempo antes de que Abbott lo haga. a los Estados Unidos De hecho, el estudio clínico acaba de concluir esta primavera, por lo que la presentación reglamentaria debería estar a punto de suceder.
Diabetes App Security: Descubrimos que el Dr. David Klonoff, fundador de Diabetes Technology Society, encabezará un nuevo Grupo de trabajo de seguridad cibernética para analizar la seguridad de las aplicaciones móviles para la diabetes. Escuchamos que cuenta con el respaldo de CMS, la FDA y Homeland Security. ¡Guauu! Más sobre eso pronto.
Y ESTO …
. Las compañías de bombas estaban haciendo un gran tadoo sobre la terapia de bomba para los tipos 2, ya que al parecer, más médicos están pensando en ello en estos días. En caso de que se lo esté preguntando, Medtronic no tenía ningún producto nuevo en ese frente; el signo es solo marketing.
* * * La nueva bomba t: flex de Tandem, por otro lado, tiene 480 unidades y IS está diseñada para los tipos 2 que necesitan más insulina. También podría ser útil para los adolescentes que necesitan más insulina debido a las hormonas de la pubertad, entendemos, aunque todavía no está aprobado por la FDA.

Este es el bolígrafo de insulina verdaderamente inteligente que desarrollan mis amigos de Companion Medical, que ahora recibe dinero de inversionistas de Eli Lilly. El lápiz tiene una inteligencia incorporada en el chip de la computadora que hace un seguimiento de su dosificación tal como lo hace una bomba de insulina, y accede a esa información en la aplicación complementaria a través del Bluetooth BLE.Ofrece cálculos de dosificación y recordatorios también. Lo veremos más de cerca pronto.

* * *
Mi buen amigo y renombrado endocrinólogo de Joslin, el Dr. Richard Jackson, dice que este nuevo medicamento para reducir el colesterol LDL, PCSK9 de Sanofi y Regeneron, "funciona increíble. "También conocido como alirocumab (nombre comercial Praluent), recién fue aprobado por la FDA el martes, y la población objetivo son pacientes que no pueden tolerar las estatinas, principalmente debido a los efectos secundarios.

Esta compañía, San Meditech, tenía configurada una pagoda completa para mostrar su CGM con Bluetooth y bajo costo que está despegando en China. Todavía no está disponible en los EE. UU., Tiene el potencial de ser producido en masa a bajo precio, lo que le da la capacidad de tecnología disruptiva que podría barrer el mercado. Solo el tiempo dirá …
* * *
Este nuevo dispositivo de Nuerometrix llamado Quell funciona para reducir el dolor de la neuropatía, la ciática y otros dolores crónicos a través de los pulsos neuronales. Recientemente fue aprobado por la FDA y recién está comenzando a llegar al mercado como una nueva y sorprendente opción sin medicamentos para el alivio del dolor. Más sobre esto pronto.
* * *

Gente real que usa la tecnología
Es notable que en las muchas sesiones, este año haya MUCHO más contenido sobre cómo usar la tecnología con éxito para ayudar a los pacientes con su autocuidado. Hubo incluso varias sesiones que se centraron en el uso y las perspectivas de los pacientes tanto en dispositivos para la diabetes como en las redes sociales, ¡lo cual fue un nuevo territorio para la reunión de la ADA! Entre ellos, hubo una sesión sobre el uso de la tecnología para mejores resultados, incluida la conferenciante del DOC Kelly Close; una sesión sobre Dispositivos y tecnología para la diabetes: la experiencia del paciente, que incluye al hablante de DOC Adam Brown; una sesión sobre Nuevas Tecnologías para el Cambio de Comportamiento, incluida la investigadora de ePatient Joyce Lee; Deb Greenwood, de AADE, habla sobre el uso de las redes sociales para la autogestión del paciente; y mi propia sesión sobre Aprovechamiento de la tecnología para mejorar los resultados de la diabetes (hablé sobre por qué las conexiones con las redes sociales son importantes).

Además de eso, esta mañana la compañía de medidores habilitada para celulares Telcare lanzó un Índice Nacional de Conciencia sobre la Diabetes que examina los costos e impactos de la diabetes y las opciones tecnológicas, junto con lo que el público general y las personas con discapacidad realmente saben sobre estos problemas. Los resultados muestran que el 52% de los estadounidenses dicen que confían en la tecnología, y ese número sube ligeramente al 57% cuando se combina con la experiencia de los profesionales de la salud. Los resultados también muestran que el 65% de las personas quiere que los médicos incorporen tecnología en sus planes de salud y el 88% quiere acceso a datos en tiempo real para nuestra gestión de D (¡no es una broma!). De todos los encuestados, las personas entre las edades de 18 y 34 años confían más en la tecnología, y el 55% de los Millennials dicen que confiarían en una aplicación de salud sobre su médico para obtener asesoramiento.
Como notado, tendremos un informe separado muy pronto sobre algunas de las ciencias presentadas en ADA 2015. ¡Así que estén atentos, fanáticos de D-News!
Descargo de responsabilidad: contenido creado por el equipo de Diabetes Mine.Para más detalles, haga clic aquí.
Descargo de responsabilidadEste contenido está creado para Diabetes Mine, un blog de salud del consumidor enfocado en la comunidad de la diabetes. El contenido no se revisa médicamente y no cumple con las pautas editoriales de Healthline. Para obtener más información sobre la asociación de Healthline con Diabetes Mine, haga clic aquí.
Otra asociación comercial: JDRF y BD se unen para mejorar el bombeo de insulina

ATTD 2015: conferencia premier sobre tecnología para la diabetes

El nuevo páncreas biónico iLet y otras noticias sobre diabetes de la Conferencia Friends for Life 2015

La conferencia anual Friends For Diabetes Friends for Life muestra nueva diabetes tecnología y tratamientos.


